Аутотрансплантат (аутографт) губчатого вещества кости у кошек и собак
Введение
Трансплантация кости была введена в гуманную хирургическую практику в конце 19-го века, и в последующие 100 лет были хорошо установлены основные принципы. Сохраненная кость (замороженная, замороженно-высушенная и облученная) пришла в общее использование в поздние 1940-е.
На сегодня, в хирургической практике у мелких домашних животных наибольшее распространение получил аутотрансплантат или аутографт губчатого вещества кости, о чем будет рассказано более подробное далее в данной статье.
Примечание. Трансплантат в английских источниках обычно именуют как «graft». Далее в тексте автор будет использовать взаимозаменяемо как графт (пр. аутографт), так и трансплантат (пр. аутотрансплантат).
Терминология
Трансплантация костной ткани – это хирургическая операция по переносу или имплантации кости (или же ее заменителей) в целях улучшения заживления на фоне различных патологий (чаще для ускорения заживления переломов).
Благотворное действие трансплантата в зоне реципиента может опосредоваться через следующие основные механизмы:
• Остеокондукция (osteoconduction) – способность остеопластического материала играть роль пассивного каркаса (матрикса) для наращивания новой ткани с последующей резорбцией имплантированного графта.
• Остеоиндукция (osteoinduction) – стимуляция и активация прилегающих мезенхимальных клеток для их дифференциации в клетки вовлеченные в рост кости, включая остеобласты и остеокласты. Данный процесс вызывается факторами роста высвобождаемыми костным трансплантатом.
• Остеогенез (osteogenesis) – формирование новой кости самим трансплантатом. Трансплантат должен содержать жизнеспособные остеобласты и откладывать остеоидные, или стволовые клетки и дифференцировать их в остеоблласты.
• Остеопродвижение (osteopromotion) – улучшение формирование кости без прямой остеоиндукции или остеокондукции. Для примера, дериваты матрикса эмали не имеют остеокондуктивных свойств, но они могут улучшать остеоиндуктивный эффект деминерализованного костного матрикса. Альтернативно, создавая сосудистое и богатое кислородом окружение позволяет возобновиться заживлению перелома.
• Остеоинтеграция (osteointegration) – процесс при котором материал трансплантата интегрируется в окружающую кость места реципиента.
Остеоиндукция, остеокондукция и остеогенез при трансплантации кости играют наиболее значимую роль, а вот остеопродвижение и остеоинтеграция – лишь незначительную.
В зависимости от источников получения кости или ее заменителей, выделяют четыре источника.
1. Аутотрансплантат (аутографт) – трансплантат, полученный от того же животного. При данном виде трансплантации одно и то же животное служит как донором, так и реципиентом. Свежий аутотрансплантат имеет максимальный остеогенный потенциал и ранний ответ. Трансплантат по своему составу может быть губчатым, кортикальным или смешанным (кортико-губчатым).
2. Аллотранслантат (аллографт) – транслантат полученный от того же вида животного. Свежий аллографт имеет остегенные, остеоиндуктивные и остеокондуктивные свойства, но он обычно отторгается иммунной системой реципиента и поэтому редко используется. При сохранении посредством замораживания и высушивания снижается антигенная стимуляция трансплантата. Главное преимущество аллографта – доступность трансплантата желаемой формы и размера, но окончательная эффективность данного вида лечения достаточно низкая.
3. Ксенотрансплантат (ксенографт) – трансплантат, полученный от животного другого вида. Данный трансплантат имеет наименьший остеогенный потенциал и наиболее вероятно вызовет реакцию на инородное тело (отторжение). Для использования данного вида трансплантата крайне мало клинических показаний.
4. Синтетические заменители костного трансплантата – синтетические материалы, используются по причине их остеокондуктивных свойств. Их матрикс дает поддержку и место присоединения формирующих кость клеток, и некоторые формы могут давать временную механическую поддержку при восстановлении перелома. Заменители костного трансплантата могут также служить как средство, доставляющее антибиотики, остеоиндуктивные факторы роста, такие как морфогенетические протеин, или клетки предшественники (остеопрогениторы).
Различные типы трансплантатов проявляют свои различные свойства, что суммировано в нижеследующей таблице:
Таблица. Характеристики различных типов костных трансплантатов
|
Тип |
Трансплантат |
Остеокондукция |
Остеоиндукция |
Остеогенез |
|
Аутотрансплантат (ауторафт) |
Губчатый |
+++ |
+++ |
+++ |
|
Кортикальный |
++ |
++ |
++ |
|
|
Аутотрансплантат – губчатый |
Свеже-замороженный |
++ |
+ |
– |
|
Свеже-высушенный |
++ |
+ |
– |
|
|
Аутотрансплантат – кортикальный |
Свеже-замороженный |
+ |
Ограничено |
– |
|
Свеже-высушенный |
+ |
Ограничено |
– |
|
|
Демиленизированный костный матрикс |
|
+ |
++ |
– |
|
Минералы |
Кальция фосфат |
+ |
– |
– |
|
Костный морфогенный протеин |
|
– |
+++ |
– |
Источник. Brinker, Piermattei and Flo's Handbook of Small Animal Orthopedics and Fracture Repair, 5th Edition.
Тип костного трансплантата должен выбираться при рассмотрении требований специфической ситуации. При достаточном количестве остеогенных клеток, представленных в зоне, что часто случается при дефекте зоны метафиза здоровой кости, только остеокондуктивного матрикса зоны перелома может оказаться достаточно. В зонах с недостатком остеогенных предшественников, таких как тяжелый костный дефект, несращение с формированием рубцовых тканей и зонах предшествующей инфекции, может потребоваться комбинация остеогенных клеток, остеокондуктивного материала и факторов остеокоиндуктивного роста.
Аутогенная губчатая кость – золотой стандарт для материала костного трансплантата и имплант выбора для большинства целей т.к. она обладает остеогенными свойствами (по причине наличия костно-формирующих клеток) и поэтому быстро обеспечивает прямое формирование кости, имеет остеоиндуктивные факторы роста и матрикс обеспечивающий формирование каркаса с большой поверхностью для ранней васкуляризации и остеокондукции. Губчатая кость – единственный имплант, который может быть безопасно применен в контаминированной зоне; сосудистое прорастания и остеокондукция в кортикальном трансплантате происходят более медленно, делая его склонным к секвестрации в инфицированных зонах.
В практике ветеринарного врача мелких домашних животных наибольшее распространение получило использование аутотрансплантата губчатого вещества, он легко собирается с места донора, легко помещается в зону реципиента и проявляет значительную эффективность в ускорении заживления костных дефектов при открытой редукции и жесткой внутренней фиксации. Далее в статье речь пойдет именно о данном виде лечения.
Показания
Показания для костной трансплантации включают в себя нижеследующее:
• Сложные переломы. Аутографт губчатого вещества способствует быстрому заживления дефекта, тем самым исключается нестабильность, которая в противном случае вызывает отказ костных имплантов. В дополнение, аутографт губчатого вещества кости, положенный вдоль анатомически реконструируемой линии переломов способствует ускорению формирования костных мостиков, повышая силы заживления кости;
• Заполнение костных дефектов остающихся после реконструкции переломов или коррективной остеотомии;
• Переломы с плохим потенциалом заживления;
• Артродез (происходит значительное ускорение формирования желаемого анкилоза);
• Межпозвоночное сращение;
• Лечение замедленного сращения или несращения переломов. Аутотрансплантация губчатого вещества используется совместно с редукцией и стабилизацией посредством внутренней фиксации. Особенно данный метод показан для биологически неактивных мест несращения. Трансплантат может эффективно использоваться при инфицированном несращении и хроническом остеомиелите. Аутографт губчатого вещества кости используется для стимуляции заживления при несращении.
• Лечение костных дефектов развивающихся при кюретаже кист кости или удалении доброкачественных опухолей посредством внесения трансплантата в зону операции.
Окончательным желаемым результатом использования аутотрансплантата является ускорение формирования мостовой мозоли (bridging callus).
Техника проведения аутотрансплантации губчатой кости у кошек и собак
Источники (донорские места) и техника забора губчатой кости
Обязательными условиями для места донора являются легкая доступность и наличие большого количества губчатого вещества. При проведении забора материала еще одним обязательным условием является строгое соблюдение правил асептики. При необходимости сбора большого количества губчатого вещества, могу использоваться несколько места для донорства. Поля получения аутотрансплантата различаются по качеству и количеству собранного материала и пропорций биологически активных клеток. У кошек и собак сравнительные характеристики трансплантатов, собранных с различных мест слабо задокументированы.
Выбор места во многом определяется исходной операцией. Наиболее частыми местами сбора аутотрансплантата губчатого вещества у кошек и собак являются нижеследующие:
• Латеральный проксимальный метафиз плечевой кости в основании большого бугра;
• Крылья подвздошной кости, дорсально или латерально;
• Медиальный проксимальный метафиз большеберцовой кости;
• Медиальный или латеральный дистальный мыщелок бедренной кости (данные источник используется достаточно редко).
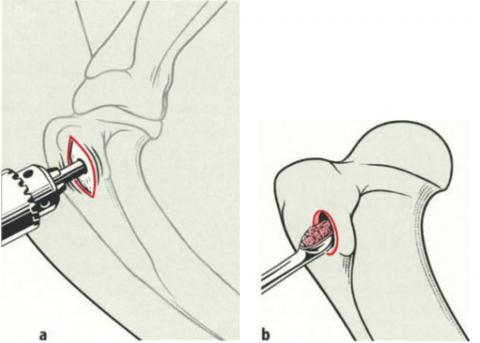
Рисунок. a,b. Большой бугор плечевой кости.
a. Кранио-латеральный кожный разрез длиною 2-3 см обнажает с обнажением периоста и каудальным отведением акромиальной части дельтовидной мышцы, затем следует разрез длиной 1-2 см с обнажением достаточной площади кости для проведения перфорации коркового вещества при помощи спицы Штеймана, сверла или трепана достаточного размера. Существуют рекомендации по использовании для плечевой кости спиц Штеймана в виде троакара с диаметром 4,8-6,4 мм.
b. При помощи острой костной кюретки должного размера губчатое вещество может быть выскоблено и собрано в чашку из нержавеющей стали или сохраняться между увлажненными кровью или раствором Рингера салфетками. Размер кюретки прямо пропорционален размеру животного и должен быть достаточно велик для легкого сбора губчатого вещества кости. Подрыв суставного хряща должен избегаться. У растущих собак, соблюдаются предосторожности для избегания физа (зоны роста) при процедуре сбора.
Источник. Manual of Internal Fixation in Small Animals 2nd Rev. Ed. (Springer, 1998)
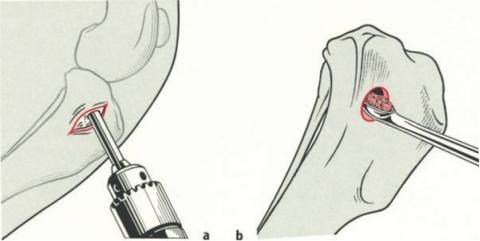
Рисунок. a,b. Проксимальный отдел большеберцовой кости.
a. Разрез кожи и подкожной клетчатки длинной 2-3 см на медиальной поверхности проксимального конца большеберцовой кости на 2-4 см ниже суставного пространства, в точке между средней и каудальной третью ширины большеберцовой кости, что обеспечивает легкий доступ к губчатому веществу.
b. В данном месте также как и с плечевой костью сбор аутографта проводится при помощи костной кюретки.
У малых пород, должны избегаться широкие отверстия и случайная перфорация противоположной стороны, т.к. в данном случае может развиться ятрогенный перелом.
Источник. Manual of Internal Fixation in Small Animals 2nd Rev. Ed. (Springer, 1998)
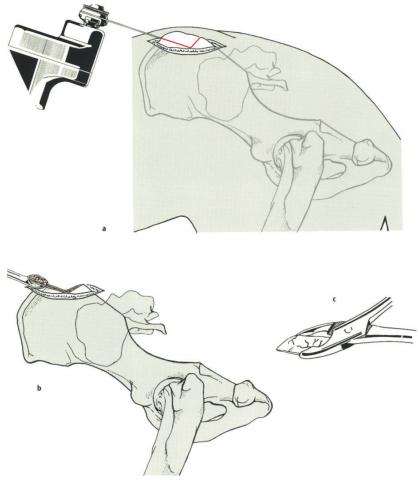
Рисунок. a-c. Крыло подвздошной кости. Дорсальный разрез через кожу и подкожные ткани над крылом подвздошной кости с последующим поднятием ягодичных мышц для обнажения краниального дорсального гребня подвздошной кости.
a. Осцилляторная пила или осцилляторный остеотом используется для удаления клина подвздошной кости. Клин кортико-губчатого раскрашивается на малые части посредством костных кусачек.
b. Костная кюретка используется для сбора губчатого вещества из тела подвздошной кости.
c. Клин кортико-губчатого вещества дробится для получения малых частей посредством костных кусачек.
Закрытие места проводится послойно посредством сближения мышц, подкожных тканей и кожи.
Источник. Manual of Internal Fixation in Small Animals 2nd Rev. Ed. (Springer, 1998)
Закрытие всех мест забора материала достигается посредством сближения подкожных тканей и кожи.
По причине комбинации легкой досягаемости и доступности достаточного костного объема, проксимальный отдел плечевой кости и большеберцовой кости используется чаще других. Одна или более зон готовится перед операцией, и драпировка позволяет проводить доступ по необходимости в период восстановления перелома. Проксимальный отдел плеча дает больше материала чем большеберцовая кость, и губчатая кость восстанавливается в зоне перелома более полно чем при использовании большеберцовой кости; второй трансплантат губчатого вещества может быть собран из плечевой кости через 8 недель, из большеберцовой кости через 12 недель после начального сбора. Послеоперационная гематома может развиться в месте донора, но может быть минимизирована бережным послойным закрытием места сбора.
Обращение с собранным материалом и его расположение
Для обеспечения оптимального выживания донорских клеток, материал кости должен трансплантироваться прямо от места донора к месту реципиента. В большинстве случаев, губчатое вещество собирается после окончания редукции и фиксации перелома и промывания места пересадки (места реципиента). Существуют преимущества при смешивании полученной губчатой кости с кровью пациента. Кровяные сгустки и формы являются формуемыми составляющими, что облегчает обращение и трансплантацию привоя в ложе реципиента. При трансплантации кости к месту опухоли или инфицированным зонам переломам, забор материала должен проводиться до проведения доступа к первичным местам или отдельной хирургической командой используя отдельный стерильный инструмент и перчатки. Кость сохраняется в марле смоченной кровью или контейнере из нержавеющей стали с аутокровью до расположения в ложе реципиента. Губчатый трансплантат не должен высыхать, не должен погружать в соль и не должен лечиться антибиотиками, т.к. вышеперечисленные процедуры токсичны для клеток. Губчатая кость свободно располагается в костных дефектах и вокруг линии перелома и удерживается на месте давлением окружающих тканей (см Рис).
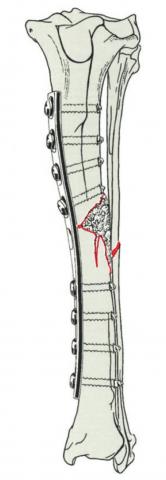
Рисунок. Кортикальный дефект. После редукции и стабилизации переломов поддерживающей пластиной в кортикальный дефект упаковывается губчатое вещество кости.
Биология
Реваскуляризация трансплантата завершается в течение 2 недель. Новая кость откладывается на трабекулярной середине трансплантата и в поверхности перелома посредством выживших остеобластов и дифференцированных мезенхимальных клеток хозяина. Происходит резорбция нектротизированной трансплатированной кости. Трансплантат полностью резорбируется и вновь сформированная кость ремоделируется в кортикальную кость в ответ на механическое раздражение через 3-6 мес. после имплантации.
Всегда следует помнить, что даже в лучшем случае, выживаемость клеток трансплантата свежего аутогенного губчатого вещества при использовании и обращении в оптимальных условиях составляет лишь 15%.
Осложнения
Аутогенный костный трансплантат вероятно служит оптимальным продуктом. Однако, аутогенная трансплантация потенциально содержит недостатки, связанные с процедурой сбора материала. Осложнения при использовании аутогенных костных трансплантатов могут включать в себя следующее:
• Требование второго хирургического поля, что повышает время операции, цену и потенциально повышает смертность.
• Формирование серомы и другие раневые нарушения в месте сбора материала.
• Боль в месте сбора аутотрансплантата – данная проблема актуальна при получении аутографта у людей, у кошек и собак не имеет существенного значения.
• Потенциальный риск перелома в зоне сбора материала.
• Заражение места сбора бактериями или злокачественными клетками.
• Косметические повреждения (рубцы в зоне сбора материала) – данная проблема также актуальна для людей, но не имеет существенного значения у кошек и собак.
Осложнение в зоне реципиента включают отказ трансплантата в стимуляции формирования кости и резорбция трансплантата.
Валерий Шубин, ветеринарный врач, г. Балаково